Витамин D как фактор восстановления мышечной ткани после спортивных тренировок
Шаблон
нутрицифтической формулы
Скелетные мышцы – пластичная ткань, обладающая способностью к адаптации и регенерации в условиях стресса и в ответ на повреждения. При чрезмерных физических нагрузках наблюдается значительное повреждение мышечных волокон с нарушением их структуры и функций [Mackey and Kjaer, 2017]. В зонах некроза скапливаются нейтрофилы и макрофаги, усиливается апоптоз и биогенез мышечных волокон – усиленный «клеточный оборот» способствует быстрому замещению поврежденных и погибших клеток здоровыми. При этом мышечное волокно образуется не полностью de novo, как в случае с большинством прочих типов клеток организма, а на базе сохраняющейся базальной мембраны [Lepper et al., 2011; Zammit et al., 2004].
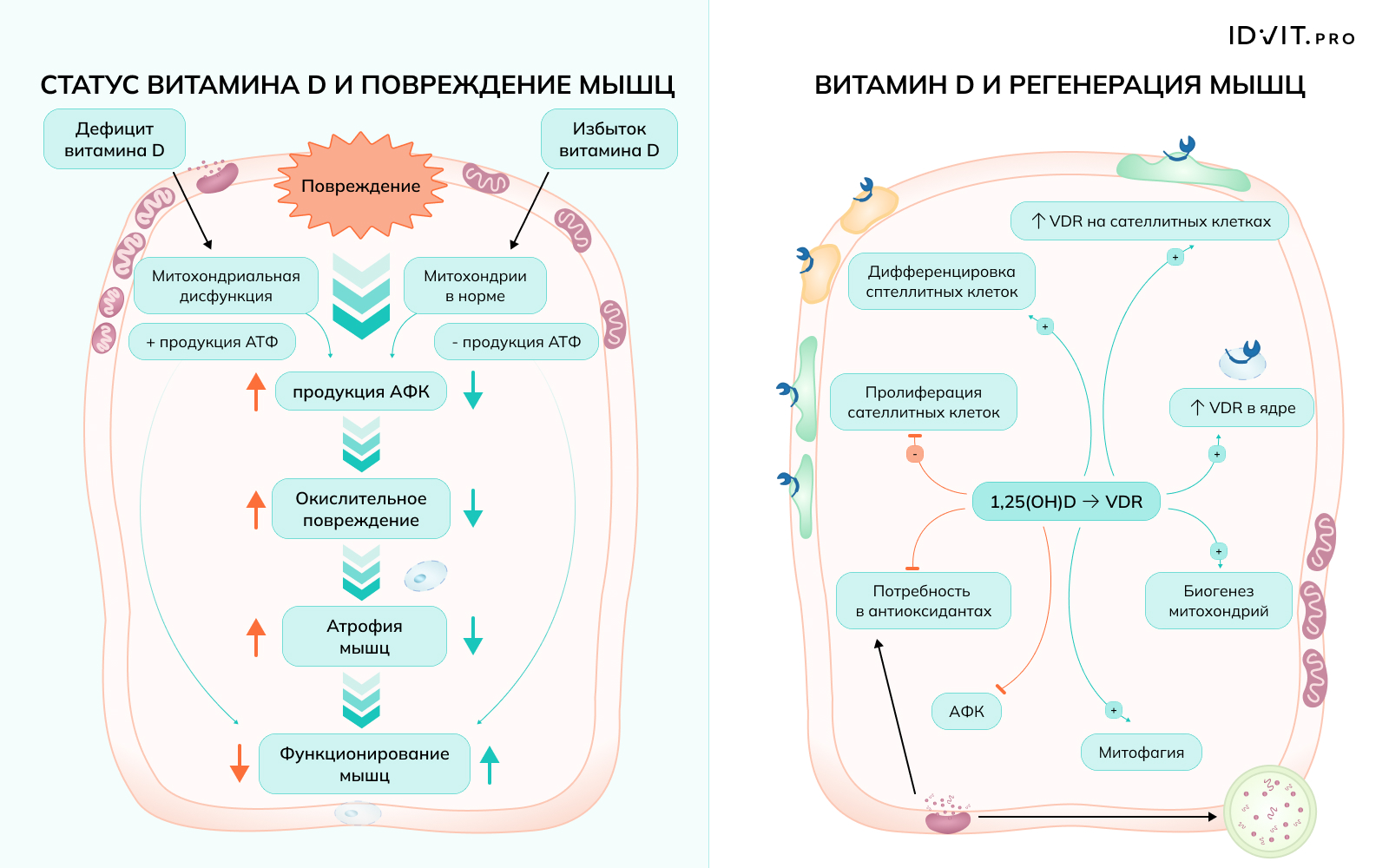
В ходе регенерации мышечной ткани усиливается экспрессия рецептора витамина D (VDR), который в норме присутствует на мембране миоцитов, как и фермент CYP27B1, превращающий 25(OH)D в его активную форму - 1,25(OH)D [Srikuea et al., 2012]. Исследования на модельных организмах показывают, что витамин D снижает выработку активных форм кислорода (АФК), увеличивает антиоксидантную емкость мышечной ткани и предотвращает окислительный стресс, который является следствием разрушения клеток мышц и сопровождает процесс регенерации мышечной ткани. Экспериментальное удаление VDR с клеток (нокдаун) приводит к снижению продукции АТФ и митохондриальной дисфункции.
Прием дополнительных количеств витамина D потенциально может стимулировать экспрессию VDR и стимулировать дифференцировку сателлитных клеток и миоцитов. Передача сигналов через VDR также увеличивает митохондриальный биогенез и передачу сигналов слияния, ингибирует выработку АФК и тем самым снижает потребность в антиоксидантах [Latham et al., 2021].
Список литературы
Пример базовой сигнатуры
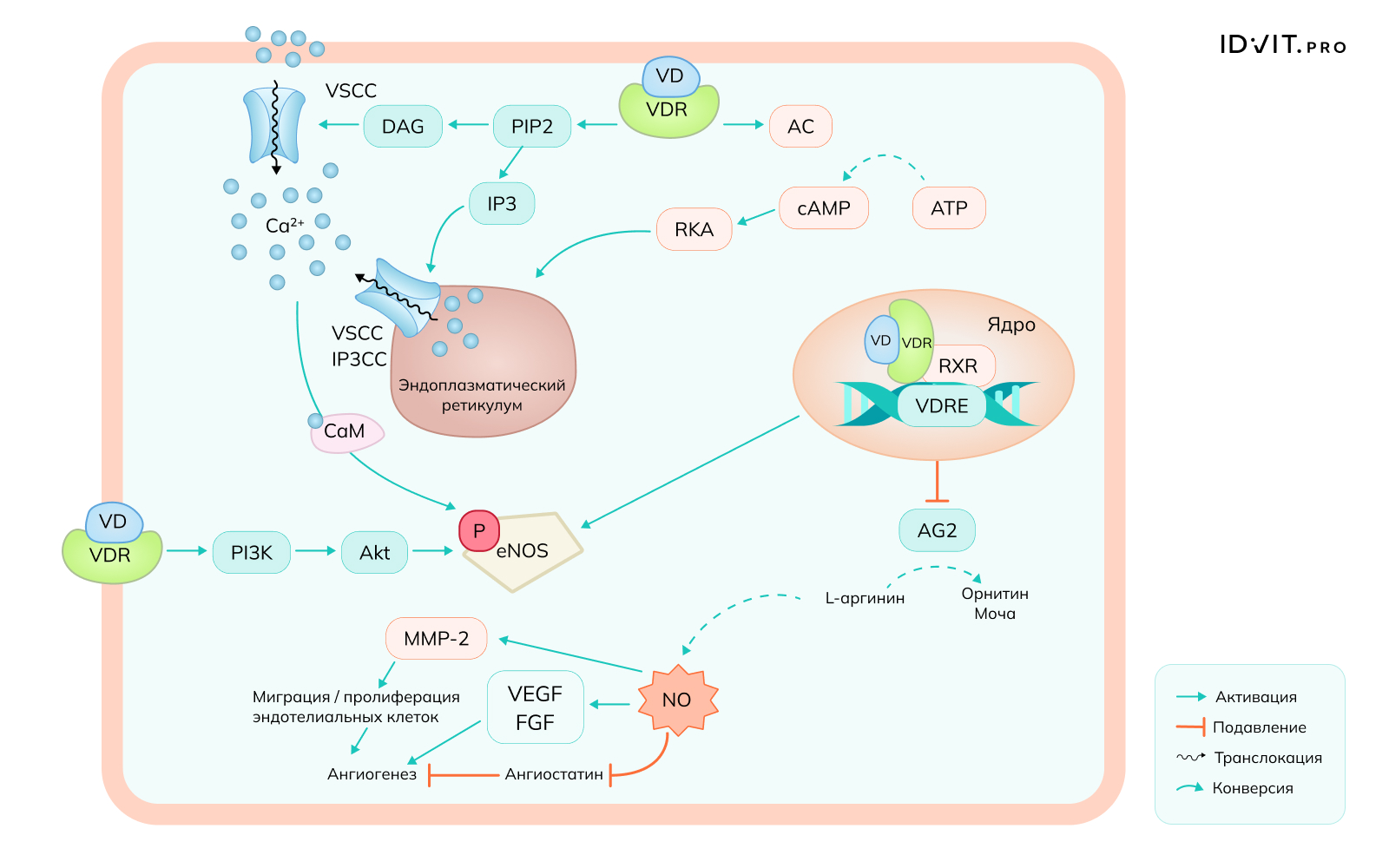
СкачатьВВитамин D и его рецептор (VDR) регулируют процесс ангиогенеза, что также имеет большое значение в процессе восстановления мышечной ткани после интенсивных спортивных тренировок. VDR влияет на активность eNOS и продукцию NO, так как способствует образованию внутриклеточных вторичных мессенджеров (аденилатциклазы, диацилглицерина и инозитолтрифосфата). Эти соединения стимулируют приток кальция и облегчают путь активации eNOS. Еще один механизм-промотор eNOS – фосфорилирование серина на молекуле фермента.
 Вход
Вход